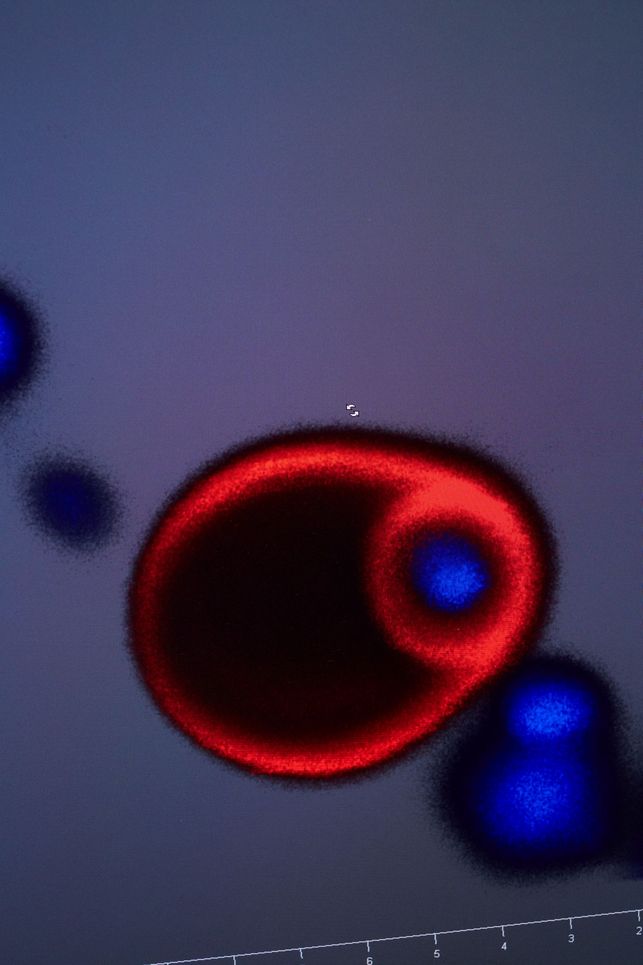
Er sieht aus wie Pac Man. Doch anders als der nimmersatte Held des Videospiels aus den 1980er Jahren frisst der Makrophage auf dem Bildschirm keine Pillen, sondern kleine Punkte: blau eingefärbte E. coli-Bakterien. Makrophagen sind Fresszellen, die im Körper Krankheitserreger aufnehmen und unschädlich machen. Der auf dem Bildschirm hat eine rot leuchtende Membran und entstand nicht, wie gewöhnlich, aus Zellen des Knochenmarks, sondern hier im Labor. Natürliche Makrophagen können viel, aber nicht alles. Deshalb gibt es Antibiotika. Da aber immer mehr Keime resistent gegen die Medikamente sind, suchen Wissenschaftler nach Alternativen. Eine davon ist der synthetische Makrophage: Eines Tages könnte er beim Job mit den Keimen helfen.
Am Rande Aachens hat sich mehr als ein Dutzend Forschungsinstitute zwischen Wiesen, Hügeln und windigen Landstraßen angesiedelt. Mittendrin steht das Leibniz-Institut für Interaktive Materialien, kurz: DWI. Ursprünglich war das DWI das »Deutsche Wollforschungsinstitut«, gegründet wurde es 1952. Sein größter Triumph der Anfangsjahre: die erste chemische Totalsynthese eines Proteins, des Insulins.
Heute beschäftigt sich das Institut mit der Erforschung und Herstellung von synthetischen Materialien, die auch komplexe Funktionen übernehmen können, wie man sie sonst nur aus der biologischen Welt kennt. Ein Fokus dieser Bemühungen sind Materialien wie Pac Man, der Kunstmakrophage: Der Natur nachempfundene Stoffe sollen eines Tages Arbeiten übernehmen, die der Körper nicht selbst verrichtet, oder als Basis für neue technische Produkte dienen.
»Noch sind wir weit davon entfernt, dass Materialien selbstständig arbeiten«, sagt Martin Möller. Der Polymerchemiker mit den lustigen Augen ist Direktor des Instituts. Große, verzweigte Moleküle sind sein Fachgebiet. »Das einzelne, kleine Molekül ist dumm«, sagt Möller, »schlauer zwar als ein Atom, aber erst Makromoleküle können echte, aktive Funktionen entwickeln. Das ist dann der Übergang vom Molekül zu einem System, das etwas leisten kann.«
Es herrscht ein eigener Geist an Möllers Institut. Um den viereckigen Hof ziehen sich die verglasten Fassaden bis hoch in den dritten Stock. Man kann überall hineinsehen, alles scheint transparent. Hier arbeiten Chemiker, Biotechnologen, Physiker und Verfahrenstechniker zusammen. Jeder bringe seine Expertise mit und lerne die Herangehensweise von Kollegen aus anderen Disziplinen kennen, erklärt Möller. Und nebenbei ihr jeweiliges Englisch.
Etwa das rasende Uruguay-Englisch von César Rodriguez-Emmenegger. Er ist der Erschaffer des synthetischen Makrophagen, der auf dem Bildschirm gerade in Echtzeit ein Bakterium verschlingt. Eines Tages soll er das im menschlichen Körper tun. »Denken Sie an Implantate, die brauchen wir Menschen ja immer häufiger, weil wir immer älter werden«, sagt Rodriguez-Emmeneger.
Auf der Oberfläche von Implantaten siedeln sich häufig Bakterien an. Die Industrie beschichtet sie heute deshalb prophylaktisch mit Antibiotika. Die wirken aber nur wenige Wochen lang, hinzukommen Resistenzen. Wenn Entzündungen entstehen, muss das Implantat entfernt werden. »Das kostet viel Geld und ist für die Patienten extrem schmerzhaft.« Mit Pac Man könnte es bleiben, wo es ist. César Rodriguez-Emmenegger würde seinen hungrigen Makrophagen losschicken. Direkt zum Entzündungsherd.
Damit die künstliche Zelle weiß, was sie dort zu fressen hat, planen die Aachener Materialforscher, sie in Zukunft mit einem ungewöhnlichen Erkennungsorgan auszustatten: DNA. »Sie ist das schlaueste Material, das wir aus der Natur kennen«, sagt Andreas Herrmann, der mit seiner Forschungsgruppe natürliche und synthetische Stoffe für medizinische Zwecke kombiniert. Die Nutzung von DNA für neue Materialfunktionen ist sein Spezialgebiet: »Wir nutzen sie als Baumaterial für komplexe Strukturen.«
In der Natur dient DNA als Träger der Erbinformation, in der Nanotechnologie ist sie eine Art Schlüsselelement. Die Paarung ihrer vier Hauptbausteine — Adenin, Thymin, Guanin und Cytosin — ermöglicht die Herstellung von Strukturen. Adenin verbindet sich immer mit Thymin, Guanin nur mit Cytosin. In vier braunen Gläsern hängen die Nukleinsäurebausteine an Andreas Herrmanns DNA-Synthesizer. Mit dem Gerät können Wissenschaftler DNA-Sequenzen aus zwölf bis 100 dieser Bausteine komponieren. Zum Vergleich: Das menschliche Genom besteht aus mehr als drei Milliarden Basenpaaren.
»Unsere Sequenzen setzen wir zum Beispiel in künstliche Vesikel ein, quasi nur die Haut von Zellen, die man dann mit Wirkstoffen befüllen kann.« Sie erhalten so einen Erkennungscode aus DNA: eine A-T-G-C-Kombination, die sich den passenden komplementären Code sucht. Dies erlaubt die gezielte Freisetzung von Stoffen oder die Fusion der Vesikel. In der Zukunft können Wirkstoffe so zielgerichtet abgegeben werden — etwa, wenn eine Biotech-Zelle an ein Bakterium andockt.

Ein weiteres Beispiel für die arbeitenden Materialien der Aachener Forscher zappelt seit Jahren im Kellerlabor des DWI. Unter dem Mikroskop erinnert es an tanzende Wesen, die wie Ringelwürmer, Schrauben oder Zopfgummis aussehen. Die Mikroschwimmer, winzige Gelpartikel, bestehen zu 80 bis 98 Prozent aus Wasser und wurden mit Nanopartikeln aus Gold bestückt. Gerade bringen die Forscher ihnen bei, sich zu bewegen. Sie beschießen sie dazu mit Laserpulsen.
Der Laser erwärmt das Gold in den Mikroschwimmern, die daraufhin in einer Schnappbewegung ihre Form verändern, bis das Licht den Bruchteil einer Sekunde später erlischt und die Schwimmer ihre ursprüngliche Form wieder einnehmen. So geht es weiter im Takt der Laserpulse. Und es entsteht Bewegung. Eines Tages könnten die Mikroschwimmer wie kleine Pumpen arbeiten, Flüssigkeiten durchmischen oder wie U-Boote durch Kapillaren tauchen, beladen mit Medikamenten. Infrarotlicht, das sie auch im Innern des Körpers erreichen könnte, würde sie dann mit Energie versorgen.
»Die Kollegen sind ganz nah dran«, sagt Martin Möller, »vielleicht brauchen sie noch ein, zwei Jahre.« In den Materialwissenschaften sei das ein Wimpernschlag. »Schließlich machen wir Grundlagenforschung, mit Betonung auf Grundlagen. Wir denken eher in Zeitfenstern von fünf bis 30 Jahren.«
Die Natur sei dabei ihre Lehrmeisterin. »Einige Aufgaben wollen wir in der Zukunft noch besser und effizienter erledigen als sie.« Das sei kein einfaches Unterfangen, schließlich habe die Natur einen Vorsprung von ein paar Milliarden Jahren. »Aus einfachen Kohlenwasserstoffverbindungen entstanden die komplexesten Moleküle und Systeme, die wir heute kennen.«
In Aachen nutzt man die Vielfalt natürlicher und synthetischer Moleküle, kombiniert sie, um voranzukommen. Schritt für Schritt tastet man sich nach vorne, um die langwierige Trial-and-Error-Methode der Evolution abzukürzen.